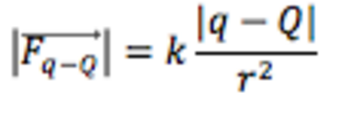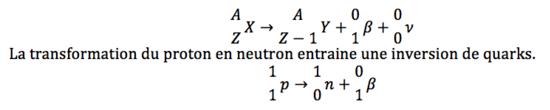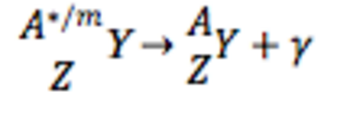-
Le noyau<o:p></o:p>
<o:p> </o:p>
<o:p> </o:p>
L’expérience de Rutherford avec la feuille d’or a montré la majorité des rayonnements α traverse<o:p></o:p>
Le noyau est positif, sa dimension est de 10-15 cm, sa densité est de 1015 g/cm3<o:p></o:p>
L’électron est négatif<o:p></o:p>
La dimension de l’atome est de 1Å = 10-10cm<o:p></o:p>
<o:p> </o:p>
I) Composition / classification<o:p></o:p>
· Nomenclature<o:p></o:p>
<o:p> </o:p>
A nucléons (Z + N)<o:p></o:p>
Z protons<o:p></o:p>
A n’a pas d’unité (nombre de nucléons), la masse atomique est en gramme, la masse réelle est en u.<o:p></o:p>
<o:p> </o:p>
· Classification chimique<o:p></o:p>
Le tableau périodique : <o:p></o:p>
Ligne 1 è lily baisa bien chez notre oncle François Nestor<o:p></o:p>
Ligne 3 è Napoléon mangea allégrement six poulets sans claquer d’argent<o:p></o:p>
Ligne 4 è Caca s’écria Titus en voyant crouler le monde<o:p></o:p>
<o:p> </o:p>
La classification physico-nucléaire se fait avec Z en abscisses et N en ordonnées<o:p></o:p>
<o:p> </o:p>
M = masse de l’atome<o:p></o:p>
M = masse du noyau (M(A,Z) - Zme)<o:p></o:p>
ΔM = défaut de masse de noyau (énergie de liaison)<o:p></o:p>
<o:p> </o:p>
· Les nucléons<o:p></o:p>
Ils sont composés de quarks u « up » (+2/3) et d « down » (-1/3)<o:p></o:p>
<o:p> </o:p>
· Classification des nuclides<o:p></o:p>
Même nombres protons : isotopes (quand instable è radio-isotope)<o:p></o:p>
Même nombres nucléons: isobares<o:p></o:p>
Même nombres neutrons: isotones<o:p></o:p>
Même nombres protons et nucléons : isomère (se différencie en énergie : le moins stable est dit métastable)<o:p></o:p>
<o:p> </o:p>
· Notion d’abondance isotopique<o:p></o:p>
3 isotopes ne pas pareillement présents dans la nature<o:p></o:p>
<o:p> </o:p>
· Noyaux stables et instables<o:p></o:p>
Les éléments lourds ont plus de neutrons que de protons.<o:p></o:p>
Quand il y a trop de neutron : β- : neutron devient proton + émission β+<o:p></o:p>
β+ : proton devient neutron + émission β-<o:p></o:p>
Quand il y a trop de proton et de neutron : α : fission spontanée + émission α<o:p></o:p>
<o:p> </o:p>
II) Défaut de masse et énergie de liaison<o:p></o:p>
M(A, Z) < Σmi = M(A, Z) + EL<o:p></o:p>
EL = 931,5 ΔM MeV<o:p></o:p>
Σmi – M(A, Z) = ΔM(A, Z)<o:p></o:p>
<o:p> </o:p>
Quand on pèse un atome, on néglige l’énergie de liaison de électrons (en keV)<o:p></o:p>
/ !\ on ne néglige pas la masse des électrons <o:p></o:p>
<o:p> </o:p>
ΔM(A, Z) ≈ ΔM(A, Z) = Zme + Zmp + (A – Z)mn – M(A, Z)<o:p></o:p>
ΔM(A, Z) = ZM(1, 1) + (A, Z)mn – M(A, Z)<o:p></o:p>
ELn = énergie de dissociation du noyau (permet la transformation de masse)<o:p></o:p>
<o:p> </o:p>
III) Facteurs de stabilité nucléaire<o:p></o:p>
· Courbe énergie de liaison par nucléons<o:p></o:p>
Le maximum d’énergie de liaisons est de 8,7 nucléons <o:p></o:p>
Plus un élément est léger plus son énergie de liaisons est faible<o:p></o:p>
Quand on arrive à un maximum d’énergie de liaison, on est à un maximum de stabilité<o:p></o:p>
On a des maxima pour les nombres dit « magiques » : 2, 8, 20, 50, 88, 126<o:p></o:p>
<o:p> </o:p>
· Graphe N = f(Z)<o:p></o:p>
La premièe bissectrice va jusqu’au calcium<o:p></o:p>
Après suivant le surplus de neutrons ou de protons on a des émissions α, β, γ.<o:p></o:p>
<o:p> </o:p>
· Parité du nombre de nucléons <o:p></o:p>
Z<o:p></o:p>
N<o:p></o:p>
A<o:p></o:p>
Nombre de noyaux stables<o:p></o:p>
Pair <o:p></o:p>
Pair<o:p></o:p>
Pair<o:p></o:p>
166<o:p></o:p>
Pair <o:p></o:p>
Impair<o:p></o:p>
Impair<o:p></o:p>
55<o:p></o:p>
Impair<o:p></o:p>
Pair<o:p></o:p>
Impair<o:p></o:p>
51<o:p></o:p>
Impair<o:p></o:p>
Impair <o:p></o:p>
Pair<o:p></o:p>
5<o:p></o:p>
Les neutrons et les protons ont des spins qui s’associe par paires et donnent un système plus stable.<o:p></o:p>
<o:p> </o:p>
IV) Forces nucléaires <o:p></o:p>
· Forces électrostatiques<o:p></o:p>
<o:p> </o:p>
· Forces nucléaires spécifiques<o:p></o:p>
Il en existe deux types :<o:p></o:p>
- Les interactions faibles : ce sont des transformations radioactives<o:p></o:p>
-Les interactions fortes : ce sont les cohésions dans le noyau<o:p></o:p>
Il y a deux protons : 1 fixe et 1 mobile<o:p></o:p>
Il y a une attraction quand le proton rentre dans le champ d’attraction : c’est un puit de potentiel.<o:p></o:p>
L’incompressibilité de la matière fait que le proton ou le neutron ne pénétre pas à l’intérieur d’un autre neutron ou proton.<o:p></o:p>
Les quarks ont une force de cohésion entre eux (dont le gluon qui est une petite particule qui assure la cohésion)<o:p></o:p>
<o:p> </o:p>
V) Modèle nucléaire<o:p></o:p>
· Modèle de la goutte sphérique<o:p></o:p>
La tension superficielle est suffisamment grande, la molécule en goutte intérieure maintenue è c’est la fission spontanée <o:p></o:p>
<o:p> </o:p>
<o:p> </o:p>
VI) Réactions de fusion et de fission nucléaire<o:p></o:p>
· Fission<o:p></o:p>
1 g d’uranium = 2 tonnes de pétrole<o:p></o:p>
On bombarde l’uranium avec des neutrons qui permet la transformation en xénon + strontium + 3 neutrons<o:p></o:p>
On va vers une stabilité quand on va vers un A de plus en plus petit.<o:p></o:p>
Plus EL est importante plus on libère de l’énergie <o:p></o:p>
Exemples : bombe A / centrale nucléaire<o:p></o:p>
<o:p> </o:p>
· Fusion<o:p></o:p>
La fusion augmente l’énergie de liaison du noyau<o:p></o:p>
On passe à un niveau supérieur après la fusion vers un A plus grand<o:p></o:p>
1 g équivaut à 12 tonnes de pétrole<o:p></o:p>
On libère 6 fois plus d’énergie qu’avec la fission<o:p></o:p>
Exemples : bombe H / ITER<o:p></o:p>
 votre commentaire
votre commentaire
-
Transformations radioactives<o:p></o:p>
<o:p> </o:p>
<o:p> </o:p>
Quand il y a une transformation radioactive, on tend vers une évolution vers une plus grande stabilité.<o:p></o:p>
L’énergie de liaison augmente avec une perte de masse.<o:p></o:p>
La libération de l’énergie se fait par émission de photon.<o:p></o:p>
À ce jour il existe 274 noyaux stables et 51 noyaux instables.<o:p></o:p>
<o:p> </o:p>
I) Historique<o:p></o:p>
Ils ont alors découvert trois types de rayonnement : α : attiré par le pole négatif
<o:p></o:p>
β : attiré par le pole positif<o:p></o:p>
γ : n’est pas dévié<o:p></o:p>
<o:p></o:p>
II) Classification<o:p></o:p>
Si il y a trop de Z et de N (quand A > 200), on a une transformation α.<o:p></o:p>
Si il y a trop de Z, on a une transformation β+ (un proton se transforme en neutron).<o:p></o:p>
Si il y a trop de N, on a une transformation β- (un neutron se transforme en proton).<o:p></o:p>
Quand il y a une modification du noyau (donc de A), on a une désexcitation spontanée γ.<o:p></o:p>
<o:p> </o:p>
α, β+, β- sont des transformations dites isobariques.<o:p></o:p>
γ est une transformation dite isomérique.<o:p></o:p>
<o:p> </o:p>
III) Évolution vers une masse inférieure<o:p></o:p>
Lors des transformations β et β, on a une perte de masse qui permet à l’atome de rejoindre une vallée de stabilité.<o:p></o:p>
Plus la masse est faible plus le noyau est stable<o:p></o:p>
 votre commentaire
votre commentaire
-
Radioactivité α<o:p></o:p>
<o:p> </o:p>
IV) Parcours dans la matière<o:p></o:p>
La particule α est lourde et lente (5% de la célérité)<o:p></o:p>
Sa trajectoire est rectiligne et emporte des électrons sur son passage et crée une ionisation de l’atome.<o:p></o:p>
La perte de l’énergie freine l’atome est crée un maximum d’ionisation.<o:p></o:p>
Quand on a un arrêt du rayonnement α, on a le pic de Bragg.<o:p></o:p>
Arrêt dans l’air : 4 cm<o:p></o:p>
Arrêt dans les tissus : 10 μm<o:p></o:p>
<o:p> </o:p>
V) Applications biomédicales<o:p></o:p>
Les rayonnements α ne sont pas dangereux car ils sont arrêtés par les tissus externes du corps.<o:p></o:p>
Mais quand ils sont absorbés, il y a un danger car le radon 222 est un émetteur α naturel, on a donc une irradiation.<o:p></o:p>
Ce radon 222 est surtout présent dan le sous sol granitique.<o:p></o:p>
Le radon peut se désintégrer jusqu’au plomb et donc entrainer soit le saturnisme, soit une intoxication au plomb soit la mort.<o:p></o:p>
Mais les rayonnements α peuvent aussi soigner le cancer.<o:p></o:p>
 votre commentaire
votre commentaire
-
Transformations isobariques<o:p></o:p>
<o:p> </o:p>
I) Définition<o:p></o:p>
Il y a conservation de A<o:p></o:p>
Quand il y a trop de proton, on a une désintégration β+<o:p></o:p>
Quand il y a trop de neutron, on a une désintégration β-<o:p></o:p>
<o:p> </o:p>
II) Désintégration β-<o:p></o:p>
· Réaction de désintégration<o:p></o:p>
<o:p> </o:p>
· Bilan masse énergie (conservation de E)<o:p></o:p>
Le défaut de masse est ΔM = M(A, Z) – M(A, Z+1) <o:p></o:p>
La masse du noyau est M(A, Z) = M(A, Z) - Zme<o:p></o:p>
<o:p> </o:p>
· Spectre en énergie (conservation de la quantité de mouvement)<o:p></o:p>
<o:p> </o:p>
· Parcours dans la matière<o:p></o:p>
Quand v > 0,9c on dit que la particule est relativiste<o:p></o:p>
Le parcours est non rectiligne<o:p></o:p>
La portée est de quelques mm<o:p></o:p>
Les particules β- sont arrêtées par une feuille de métal<o:p></o:p>
<o:p> </o:p>
· Applications biomédicales : iode 131<o:p></o:p>
L’iode 131 est un émetteur β- avec une demi-vie de 8 jour et une énergie maximum de Emax = 606 keV<o:p></o:p>
Il provient de l’écorce terrestre, du produit de la fission nucléaire<o:p></o:p>
Il est produit pour une utilisation médicale<o:p></o:p>
La radioprotection concernant les sources externes est un écran simple<o:p></o:p>
La radioprotection concernant les sources internes est l’iode qui est concentrée vers la thyroïde <o:p></o:p>
La radiothérapie est métabolique è pour le traitement du cancer on utilise l’iode qui tue les métastases des cellules thyroïdiennes
Pour l’hyperthyroïdie nodulaire ou diffuse on détruit les cellules de la thyroïde
<o:p></o:p>
<o:p> </o:p>
III) Désintégration β+<o:p></o:p>
· Réactions de désintégration
<o:p> </o:p>
· Bilan masse énergie (conservation de E)<o:p></o:p>
Il existe un seuil d’émission β+ de 1,022 MeV<o:p></o:p>
Le défaut de masse est ΔM = M(A, Z) – M(A, Z-1) – 2me<o:p></o:p>
<o:p> </o:p>
· Spectre en énergie<o:p></o:p>
Même que celui de β-<o:p></o:p>
<o:p> </o:p>
· Parcours dans la matière<o:p></o:p>
β+ entre vite en collision avec l’électron, ce qui produit un épuisement cinétique.<o:p></o:p>
On a alors une réaction particule/antiparticule è annihilation<o:p></o:p>
<o:p> </o:p>
· Applications biomédicales : Fluor 18<o:p></o:p>
- Radioprotection : On se protège des photons de 511 KeV<o:p></o:p>
On fait des tomographie par électron de position (permet repérage annihilation et métastases)<o:p></o:p>
- Utilisation en cancérologie : Les cellules cancéreuses consomme beaucoup de sucre et le fluor 18 permet de fixer le sucre.<o:p></o:p>
<o:p> </o:p>
IV) Désintégration par capture électronique (CE)<o:p></o:p>
· Réactions de désintégration
<o:p> </o:p>
· Bilan masse énergie (conservation de E)<o:p></o:p>
Le défaut de masse est ΔM = M(A, Z) – M(A, Z+1) <o:p></o:p>
Pour que la réaction soit possible il faut que ΔM > Wk (1,022 MeV) sinon β+ et CE sont en compétition<o:p></o:p>
<o:p> </o:p>
· Spectre en énergie
<o:p></o:p>
il peut y avoir émission d’un photon de fluorescence<o:p></o:p>
<o:p> </o:p>
· Applications biomédicales<o:p></o:p>
Le thallium 201 permet de réaliser des scintigraphies cardiaques è permet de voir si un produit (donc le sang) se diffuse bien ou pas <o:p></o:p>
 votre commentaire
votre commentaire
-
Transformation isomérique<o:p></o:p>
<o:p> </o:p>
<o:p> </o:p>
I) Définition<o:p></o:p>
Il n’y a pas de changement de noyau.<o:p></o:p>
Les transformations se sont par rapport aux niveaux d’énergie des nucléons.<o:p></o:p>
L’excédent d’énergie entraine l’émission d’un photon γ ou une conversion interne (noté * ou m)<o:p></o:p>
<o:p> </o:p>
II) Radioactivité γ<o:p></o:p>
· Réaction de désintégration (conservation de A et de Z)<o:p></o:p>
<o:p> </o:p>
· Bilan masse énergie (conservation de E)<o:p></o:p>
Le défaut de masse est ΔM = M(Am, Z) – M(A, Z) <o:p></o:p>
Ed = ΔM * 931,5 = Eγ<o:p></o:p>
<o:p> </o:p>
· Spectre en énergie (conservation de la quantité de mouvement)<o:p></o:p>
Ed = hν<o:p></o:p>
On obtient un spectre électromagnétique avec un spectre de raie<o:p></o:p>
<o:p> </o:p>
· Parcours dans la matière<o:p></o:p>
γ n’a pas de charge et pas d’interaction obligatoire avec la matière.<o:p></o:p>
On a une ionisation par collision avec électrons par effet Compton / effet photoélectrique / création de paires.<o:p></o:p>
γ parcours plusieurs mètres avec d’être atténués : N(x) = N(0) e-μx<o:p></o:p>
<o:p> </o:p>
· Application biomédicale : la γ-caméra<o:p></o:p>
γ fait un long parcours dans les tissus.<o:p></o:p>
On effectue alors des scintigraphie : les photons γ se transforme en photons lumineux<o:p></o:p>
La γ-caméra est un détecteur de rayonnement contrairement au scanner qui est un émetteur de rayonnement<o:p></o:p>
<o:p> </o:p>
III) Conversion interne<o:p></o:p>
· Réaction de désintégration (conservation de A et de Z)<o:p></o:p>
m ou * = métastable ou excité<o:p></o:p>
C’est l’énergie en excès directement transmise à l’électron d’un atome ionisé<o:p></o:p>
<o:p> </o:p>
· Bilan masse énergie (conservation de E)<o:p></o:p>
Le défaut de masse est ΔM = M(Am, Z) – M(A, Z) <o:p></o:p>
Ed = ΔM * 931,5 = Eγ<o:p></o:p>
<o:p> </o:p>
· Spectre en énergie (conservation de la quantité de mouvement)<o:p></o:p>
Il n’y a pas de spectre nucléaire mais un spectre de raies et continu.<o:p></o:p>
Il apparaît donc des raies de transition K et L<o:p></o:p>
Le spectre complet est le spectre continu β- + les raies de la conversion interne + la possibilité d’émission Auger.<o:p></o:p>
<o:p> </o:p>
IV) Conclusion<o:p></o:p>
Le schéma de désintégration est très complexe.<o:p></o:p>
La probabilité d’une transition de désintégration est plus ou moins importante et plus ou moins plusieurs étapes.<o:p></o:p>
On diagnostique mieux les γ pures qui sont moins irradiantes.<o:p></o:p>
<o:p> </o:p>
<o:p> </o:p>
<o:p> </o:p>
<o:p> </o:p>
Les possibilités de transition :<o:p></o:p>
α pure<o:p></o:p>
α puis γ<o:p></o:p>
β- ou β+ pure <o:p></o:p>
β- ou β+ puis γ<o:p></o:p>
γ pure<o:p></o:p>
<o:p> </o:p>
Les rayons X sont d’origine atomique <o:p></o:p>
Les rayons γ sont d’origine nucléaire<o:p></o:p>
<o:p> </o:p>
Les rayons sont arrêtés ou atténués à ces distances :<o:p></o:p>
- α è 10 μm<o:p></o:p>
- β- è quelques mm<o:p></o:p>
- β+ è 1mm + 2 photons d’annihilation <o:p></o:p>
- γ è atténués à partir de quelques mètres<o:p></o:p>
 votre commentaire
votre commentaire